Abstract
Introduzione
In tutto il mondo, si stima che circa 19 milioni di bambini abbiano un deficit visivo (definito come acuità visiva di Snellen di <6/12 [o <20/40] nell’occhio che vede meglio). La menomazione visiva può avere un profondo effetto sullo sviluppo dei bambini, sulla qualità della vita, sul livello di istruzione e sulla produttività economica.1, 2 La causa principale della menomazione della vista nei bambini è l’errore refrattivo non corretto, che colpisce circa 12 milioni di bambini, che può essere facilmente corretto con gli occhiali.3 Molti bambini in età scolare sono ostacolati dalla scarsa vista per mancanza di questo semplice intervento. La maggior parte dei bambini con problemi alla vista vive in paesi a basso reddito.4 In Kenya, per esempio, la prevalenza stimata di disabilità visiva tra i bambini in età scolare (6-20 anni) varia dal 4-8% al 5-6%.5, 6 Nelle popolazioni asiatiche, le stime vanno dal 6-4% al 22-3%.7, 8
Affrontare la cecità infantile e i danni alla vista è una delle principali priorità di VISION2020, un programma globale di lotta contro la cecità evitabile guidato dall’OMS e dall’Agenzia internazionale per la prevenzione della cecità.9 Per ridurre la cecità infantile, il programma promuove lo screening della vista di tutti i bambini che vanno a scuola e promuove l’integrazione dello screening della vista nei programmi sanitari scolastici entro il 2020. Il test della vista per identificare i bambini con disabilità visive correggibili consente di offrire interventi precoci, prima che il progresso educativo e sociale ne risenta negativamente.10
Ricerca nel contestoEvidenzaprima di questo studioUnarevisione sistematica delle applicazioni di salute mobile (mHealth) per il test della vista ha identificato numerose applicazioni disponibili; tuttavia, pochissime sono state sottoposte a convalida o certificazione. I sistemi mHealth hanno dimostrato di essere promettenti per migliorare la fornitura di assistenza sanitaria, anche se non sono state pubblicate prove di interventi mHealth per migliorare la salute degli occhi.Valore aggiunto di questo studio Questostudio ha mostrato sia la fattibilità di un efficace trasferimento di compiti agli insegnanti che utilizzano il sistema di salute degli occhi della scuola Peek per identificare e refertare i bambini con problemi di vista, sia un sostanziale aumento dell’aderenza al referral (entro 8 settimane dallo screening) di quelli identificati stabilendo un anello chiuso tra gli screener (insegnanti) e il fornitore di servizi (ospedale).Implicazioni di tutti gli elementi di prova disponibili La scarsavista ha conseguenze negative sul piano sociale, sanitario, educativo ed economico. L’identificazione precoce e il trattamento delle patologie oculari riduce la prevalenza di disturbi della vista. I nostri risultati hanno dimostrato che il sistema di salute degli occhi della scuola Peek, quando viene utilizzato dagli insegnanti, è efficace per l’identificazione e il referral, oltre a fornire i dati del sistema sanitario in tempo reale con le prove delle barriere che ostacolano l’erogazione del servizio. Le lezioni apprese da questa sperimentazione sono state adottate e ampliate in Kenya dai Ministeri della Salute e dell’Educazione fino ad arrivare a un programma su scala nazionale che serve 200.000 bambini. Inoltre, questo programma è stato replicato e ulteriormente sviluppato in India e in Botswana, che lo sta portando su scala nazionale.
Lo screening della vista dei bambini in Kenya è guidato dalle politiche scolastiche.11 Nelle aree con programmi attivi, i funzionari clinici ospedalieri addestrati e le infermiere oftalmiche di solito effettuano lo screening nelle scuole. Questa procedura richiede agli operatori oculistici di lasciare il loro abituale posto di lavoro (cliniche oculistiche ospedaliere), riducendo così la disponibilità di questi servizi. In un programma pilota di screening scolastico nella Contea di Trans Nzoia, in Kenya, abbiamo formato gli insegnanti scolastici per identificare i bambini con disabilità visive utilizzando una tessera Snellen Tumbling-E. I bambini hanno superato o non hanno superato due livelli di soglia predefiniti: 6/60 (20/200) e 6/12 (20/40), in entrambi gli occhi. Per i bambini che hanno fallito in entrambi i livelli è stata effettuata una visita in ospedale inviando una lettera al genitore o al tutore del bambino per spiegare la necessità di accedere alle cure. Tuttavia, solo pochi bambini hanno partecipato a questo ricovero ospedaliero. Le barriere multiple all’assistenza includono l’incapacità di comunicazione tra gli alunni o le scuole e i genitori o chi si prende cura di loro, così come tra le scuole o chi si prende cura di loro e gli ospedali, l’inaccessibilità dei servizi, i costi diretti e indiretti, i miti legati alle cure e la paura.12
L’accesso a un dispositivo mobile collegato nell’Africa subsahariana è aumentato drasticamente negli ultimi anni, dall’1% nel 2002 a circa il 75% nel 2016.13, 14 Questo aumento dell’utilizzo sta portando a profondi miglioramenti nella comunicazione e nel commercio, e apre nuove opportunità per l’assistenza sanitaria. L’uso di interventi di salute mobile (mHealth) a sostegno della comunicazione tra fornitori e pazienti attraverso servizi di messaggistica breve (SMS) può promuovere l’accesso all’assistenza sanitaria.15 In precedenza, abbiamo sviluppato e testato un’applicazione per smartphone per il Tumbling-E visual acuity test (Peek Acuity app) per misurare l’acuità visiva negli adulti in Kenya. Questo test era accurato e ripetibile, e accettabile per i pazienti, gli esaminatori e le parti interessate.16, 17 Abbiamo ora integrato questa app in un sistema mHealth per lo screening della vista tra i bambini in età scolare. Gli obiettivi di questo studio erano di convalidare il sistema di salute degli occhi delle scuole Peek e di valutare l’effetto di questo sistema sul tasso di riferimento dei bambini con disabilità visiva rispetto al sistema di screening visivo standard attualmente utilizzato in Kenya.
Metodi
Progettazione dello studio e partecipanti
Per prima cosa abbiamo fatto uno studio di validazione per confermare che gli insegnanti potevano essere addestrati ad effettuare lo screening della vista. Abbiamo confrontato le prestazioni sia della scheda Snellen Tumbling-E che del test Peek Acuity con un diagramma visivo standard retroilluminato EDTRS LogMAR Tumbling-E (Precision Vision, Woodstock, IL, USA) nella misurazione dell’acuità visiva nei bambini. L’ordine delle valutazioni era casuale. Questo studio di validazione è stato condotto in tre scuole non coinvolte nella prova successiva.
Abbiamo quindi condotto uno studio controllato a gruppi paralleli, a maschera singola, in 50 scuole primarie della contea di Trans Nzoia, in Kenya. I cluster erano scuole individuali senza un programma di screening visivo attivo. I bambini delle scuole sono stati sottoposti a test di disabilità visiva da parte di insegnanti che sono stati addestrati a utilizzare il sistema di screening scolastico standard Snellen Tumbling-E card e carta di riferimento) o il sistema di salute degli occhi della scuola Peek. Sono state seguite le linee guida del CONSORT per la segnalazione di studi randomizzati a grappolo.18
Tutti gli alunni che hanno frequentato gli anni 1-8 nelle scuole selezionate erano idonei all’inclusione. Ai bambini sono state fornite informazioni e moduli di consenso da dare ai genitori o ai tutori, ai quali è stato poi chiesto di dare il consenso informato per iscritto agli insegnanti per testare la vista prima dell’iscrizione. I bambini sono stati esclusi se non erano disposti o non erano in grado di dare il consenso verbale, o se i loro genitori o tutori non hanno fornito il consenso.
Lo studio è stato approvato dalla Moi University Institutional Research and Ethics Committee, Kenya e dalla London School of Hygiene & Tropical Medicine Ethics Committee, Regno Unito. L’autorizzazione è stata concessa anche dalle autorità per l’istruzione e la sanità della Trans Nzoia, Kenya. Lo studio ha aderito ai principi della Dichiarazione di Helsinki sull’etica.
Randomizzazione e mascheramento
Le scuole sono state assegnate in modo casuale (1:1) al sistema di salute degli occhi della scuola Peek (gruppo Peek) o al sistema di screening scolastico standard (gruppo standard). Sono state ottenute le coordinate geografiche di tutte le scuole idonee. Per ridurre al minimo lo squilibrio nella posizione geografica tra i due gruppi, uno statistico ha utilizzato un algoritmo basato sulla minimizzazione in R basato sulla posizione geografica (sei zone, ognuna delle quali copre 60 gradi di cerchio intorno all’ospedale di Kitale) delle scuole e la loro distanza dall’ospedale, utilizzando blocchi casuali permutati.19, 20 Utilizzando questo algoritmo di bilanciamento, abbiamo ottenuto un insieme di assegnazioni ottimali e abbiamo campionato la distribuzione finale delle assegnazioni da questo insieme di assegnazioni ottimali.
Non abbiamo potuto mascherare il gruppo di studio che fornisce la formazione, né mascherare i partecipanti e gli insegnanti al metodo di screening utilizzato. I dati primari dei risultati sono stati raccolti da un impiegato dell’ospedale che è stato mascherato al metodo di screening utilizzato. All’arrivo in ospedale, il genitore o il tutore del bambino ha presentato un documento di riferimento, identico per ogni gruppo. I bambini che hanno partecipato all’appuntamento in ospedale nel gruppo Peek sono stati contrassegnati come assistiti nell’app dell’ospedale da un impiegato diverso da quello che li ha ricevuti alla reception, per mantenere il mascheramento della raccolta dei dati primari di esito.
Procedure
Abbiamo selezionato 25 insegnanti, che in precedenza erano stati formati per utilizzare il sistema standard come parte del programma pilota di screening scolastico, in base alla loro disponibilità e all’attività svolta durante il pilota. Li abbiamo addestrati per 1 settimana su come usare uno smartphone e su come screenare e fare riferimento utilizzando entrambi i metodi (Peek e standard). Abbiamo assegnato gli insegnanti e li abbiamo trasportati nelle scuole, dove non hanno lavorato, in modo da garantire che un insegnante fosse proiettato in due scuole a testa, una per ogni gruppo. Gli insegnanti controllavano i bambini classe per classe. Abbiamo classificato i bambini negli anni 1-3 come scuola elementare inferiore e quelli negli anni 4-8 come scuola elementare superiore. Abbiamo registrato l’età, il sesso e il livello di istruzione di ogni bambino nello studio. Per coloro che sono risultati positivi (cioè non hanno potuto vedere il 6/12 in nessuno dei due occhi), abbiamo raccolto ulteriori informazioni per il contatto e il follow-up: nome del bambino, nome del genitore, lingua primaria e numero di contatto.
Nelle scuole assegnate al gruppo standard, l’insegnante ha testato la vista dei bambini per ogni occhio separatamente. L’occhio non testato è stato coperto con un occlusore. Al bambino è stata mostrata una scheda di screening della vista Tumbling-E(figura 1A) ad una distanza di 3 m. Questa scheda ha una fila di cinque lettere Es, in quattro diversi orientamenti. La dimensione delle lettere a questa distanza di prova corrisponde ad un’acuità visiva di 6/12. Il bambino ha superato il test di soglia 6/12 se ha identificato correttamente la direzione di quattro delle cinque lettere Es. Se non ha superato il test a 6/12, gli è stata mostrata la carta 6/60, che ha la lettera Es più grande, e di nuovo superato se quattro delle cinque lettere sono state identificate correttamente. Il risultato è stato registrato per ogni occhio separatamente come: può vedere 6/12, non può vedere 6/12 ma vede 6/60, o non può vedere 6/60. I bambini che non riuscivano a vedere 6/12 in entrambi gli occhi sono stati indirizzati all’ospedale di Kitale. Il modulo di riferimento cartaceo è stato compilato in triplice copia: una copia è stata data al bambino, consigliando al genitore di portare il bambino in ospedale, una copia al direttore della scuola e una copia è stata inviata direttamente all’ospedale.Figura 1Metodi di screening visivi utilizzati nei bambini in età scolare(A) Screening standard con una tessera Tumbling-E. (B) Applicazione di screening Peek Acuity utilizzata su uno smartphone. (C) Scheda di riferimento Peek che mostra la visione del bambino e le istruzioni di riferimento. (D) Genitore che riceve un messaggio SMS con le istruzioni dopo lo screening. SMS=servizio messaggi brevi.
Nelle scuole assegnate al sistema di salute degli occhi della scuola Peek school eye health system, l’insegnante ha utilizzato l’applicazione di screening visivo Peek Acuity su uno smartphone (Samsung Galaxy S3) a 2 m. Ogni occhio è stato testato separatamente, con l’occhio del collega coperto da un occlusore. Una serie di fino a cinque optotipi Tumbling-E di dimensioni equivalenti a Snellen 6/12 (20/40, LogMar 0.3) sono stati presentati in modo casuale in uno dei quattro orientamenti(figura 1B). Il bambino ha puntato nella direzione in cui ha percepito che le braccia della lettera E erano rivolte, e l’insegnante ha usato il touch screen del telefono per scorrere nella stessa direzione per inserire la risposta del bambino, senza guardare lo schermo del telefono. È stato presentato un optotipo alla volta. Il test si è concluso automaticamente quando è stato raggiunto il numero limite di passaggi (quattro su cinque) o di fallimenti (due su cinque) alla dimensione 6/12 dell’optotipo.16 Se il bambino non superava il livello 6/12, l’app presentava automaticamente un optotipo di dimensione 6/60 e il test veniva ripetuto per determinare se 6/60 (20/200, LogMAR 1.0) poteva essere visto o meno. Alla fine del test, se il bambino non ha superato il livello 6/12 in uno dei due occhi (cioè è risultato positivo allo screening), l’app ha richiesto la raccolta dei dettagli del referral (nome del paziente o del tutore, lingua locale e numero di cellulare) e ha generato un referral all’ospedale. Ad un bambino che ha ricevuto un riscontro positivo è stata data una scheda fotografica stampata con il suo nome, i dettagli di contatto dell’ospedale e gli orari di apertura da portare a casa. La tessera comprendeva un’immagine divisa con una metà sfocata nella stessa misura della disabilità visiva del bambino(figura 1C). Una volta collegata a Internet, l’applicazione invia questi dati di riferimento a un server basato su cloud, che genera automaticamente un SMS personalizzato che viene poi inviato al genitore o al tutore del bambino con consigli sull’esito della valutazione oculistica e istruzioni per il riferimento nella lingua locale scelta(figura 1D). Anche una persona di contatto (di solito il preside della scuola) ha ricevuto un SMS con l’elenco dei bambini trovati non vedenti che hanno bisogno di essere indirizzati. I messaggi sono stati inviati a intervalli di 2 settimane fino a quando il bambino non è stato ricoverato in ospedale o per un massimo di 8 settimane. Un rinvio è stato anche inviato automaticamente all’ospedale, dove una banca dati di bambini rinviati è stata tenuta accessibile attraverso un’applicazione di accoglienza ospedaliera.
Il periodo di follow-up di questa sperimentazione era di 8 settimane. Al momento della presentazione al reparto oculistico dell’ospedale di Kitale per la valutazione, un impiegato ha registrato le presenze del bambino inviato. Il team clinico ha valutato il bambino per determinare il livello di vista, la causa della menomazione della vista e le eventuali cure necessarie. Gli interventi comprendevano la fornitura di collirio, occhiali o interventi chirurgici. L’équipe ha valutato l’acutezza visiva utilizzando un grafico di Snellen di 6 m e ha classificato la causa della perdita della vista sulla base di cause comuni curabili o prevenibili.21 Tutti i bambini con problemi alla vista sono stati curati gratuitamente in ospedale.

Figura 1.Metodi di screening della vista utilizzati nei bambini in età scolare(A) Schermatura standard con una scheda Tumbling-E. (B) Applicazione di screening Peek Acuity utilizzata su uno smartphone. (C) Scheda di riferimento Peek che mostra la visione del bambino e le istruzioni di riferimento. (D) Genitore che riceve un messaggio SMS con le istruzioni dopo lo screening. SMS=servizio messaggi brevi.
Risultati
Il risultato principale, che è stato valutato a livello centrale, è stata la percentuale di partecipanti che hanno frequentato il reparto oculistico dell’ospedale di Kitale entro 8 settimane dal deferimento. Il principale risultato secondario è stato il tempo impiegato dai bambini con problemi alla vista per raggiungere l’ospedale. Riportiamo anche il livello di vista misurato in ospedale e le cause della menomazione visiva identificate.
Analisi statistica
Abbiamo calcolato la dimensione del campione ipotizzando una prevalenza di disabilità visiva del 4-8% (<6/18 nell’occhio migliore) e una media scolastica di 542 alunni (circa 25 bambini ipovedenti per scuola).5 Supponendo un effetto di disegno di 1-24 (cioè, coefficiente di correlazione intraclasse 0-01) sono state richieste almeno 21 scuole in ogni gruppo per fornire l’80% di potenza per rilevare una differenza del 10% (60% nel gruppo Peek vs 50% nel gruppo standard) nella frequenza complessiva dell’ospedale entro 8 settimane. Tuttavia, per garantire il mantenimento di una potenza sufficiente a rilevare questa differenza nel caso in cui alcune scuole avessero abbandonato lo studio, abbiamo selezionato un campione finale di 50 scuole (25 in ogni gruppo), fornendo l’88% di potenza per rilevare questa differenza se tutte le scuole hanno partecipato.
Per lo studio di validazione iniziale, abbiamo definito un bambino come ipovedente se aveva almeno un occhio classificato come ipovedente peggiore di 6/12 (o peggiore di 0-3 quando si usa LogMAR). Utilizzando ETDRS LogMAR come test di riferimento, e la precedente definizione di disabilità visiva come risultato, abbiamo stimato la sensibilità, la specificità, il valore predittivo positivo e il valore predittivo negativo per le carte Peek e Tumbling-E.
L’analisi è stata effettuata con l’intenzione di trattare. Per l’analisi primaria dell’esito, abbiamo utilizzato la regressione logistica ad effetto misto per stimare il rapporto delle probabilità (OR), confrontando le probabilità di partecipazione entro 8 settimane dal referral tra i gruppi di controllo (standard) e di intervento (Peek), prima non aggiustate e poi, in caso di squilibrio demografico tra i due gruppi, aggiustate per età, sesso, livello di istruzione e distanza dall’ospedale.
Abbiamo generato le curve di sopravvivenza di Kaplan-Meier (K-M) per illustrare la differenza di tempo di permanenza tra i due gruppi. Abbiamo valutato la differenza nel tempo di frequenza con i rapporti di rischio (HR) stimati dalla regressione di Cox, con una fragilità condivisa a livello scolastico, prima non corretta e poi regolata in base all’età, al sesso, al livello di istruzione e alla distanza dall’ospedale. Abbiamo controllato i residui di Schoenfeld e abbiamo fatto un test di proporzionalità dei pericoli per identificare se l’assunzione dei pericoli proporzionali era valida.22 In caso di violazione dell’ipotesi di rischio proporzionale, abbiamo stimato le risorse umane per fasce temporali più ristrette, entro le quali è valida l’ipotesi di rischio proporzionale. Abbiamo valutato in modo descrittivo la relazione tra il livello di visione e la diagnosi in ospedale. Per l’analisi abbiamo utilizzato la versione STATA 13 (STATA Corp, TX, USA).
Lo studio è stato registrato presso il Pan African Clinical Trial Registry, numero PACTR201503001049236.
Ruolo della fonte di finanziamento
I finanziatori dello studio non hanno avuto alcun ruolo nella progettazione dello studio, nella raccolta dei dati, nell’analisi dei dati, nell’interpretazione dei dati o nella stesura del rapporto. L’autore corrispondente aveva pieno accesso a tutti i dati dello studio e aveva la responsabilità finale della decisione di presentare il rapporto per la pubblicazione.
Risultati
Nello studio di validazione, abbiamo testato l’acuità visiva di 1862 bambini utilizzando Peek Acuity, la carta standard Tumbling-E, e ETDRS LogMAR (il test di riferimento). La prevalenza della disabilità visiva, misurata dall’ETDRS LogMAR (almeno un occhio con vista <6/12), è stata del 4% (n=65). Peek ha correttamente identificato 50 bambini su 65 come ipovedenti (sensibilità 76-9% [95% CI 64-8-86-5]) e le carte E standard hanno rilevato 49 bambini su 65 (sensibilità 75-4% [63-1-85-2]) (tabella 1). 12 (80%) di 15 bambini con disabilità visiva non identificata da Peek avevano un punteggio LogMAR nell’occhio peggiore di meno di 0-3 e migliore o uguale a 0-4. Con le carte E standard, 15 (94%) di 16 bambini rientravano in questa regione di lieve disabilità visiva, suggerendo che erano per lo più bambini con disabilità visiva più lieve ad essere mancati dalle carte Peek ed E. La specificità di Peek era inferiore (91%) a quella delle carte E standard (97%). Peek aveva un valore predittivo positivo inferiore (23% [95% CI 17-7-29-4]) rispetto alla carta E (52% [95% CI 41-1-62-0]) a causa della minore specificità di Peek (tabella 1).Tabella 1Performance di ogni test di disabilità visiva nello studio di convalidaNumero dibambini che non hanno superato il test 6/12*testin almeno un occhio (N=1862)SensibilitàSpecificitàValore predittivopositivoValore predittivo negativoLogMAR† 65 (4%)…………….Standard‡ 95 (5%)75-4% (63-1-85-2)97-4% (96-6-98-1)51-6% (41-1-62-0)99-1% (98-5-99-5)Peek‡ 216 (12%)76·9% (64·8–86·5)90·8% (89·3–92·1)23·1% (17-7-29-4)99-1% (98-5-99-5)I dati sono n (%) o % (95% CI).*Valore logaritmico 0-3.†Test eseguito dal medico oftalmologo.‡Test eseguito dall’insegnante.
Il reclutamento di prova è avvenuto tra il 2 marzo 2015 e il 13 marzo 2015. L’ultimo periodo di follow-up di 8 settimane è terminato l’8 maggio 2015. Delle 320 scuole elementari pubbliche, 25 sono state escluse in quanto già dotate di programmi attivi di screening scolastico. Delle rimanenti 295 scuole ammissibili, 50 sono state selezionate a caso e 25 sono state assegnate a ciascun gruppo(figura 2). Le distanze medie tra le scuole in cui si è svolto lo screening e l’ospedale e le dimensioni delle scuole erano simili in ogni gruppo(tabella 2). Tutti i 27316 bambini potenzialmente idonei che hanno frequentato le 50 scuole sono stati invitati a sottoporsi allo screening della vista. Il consenso dei genitori e il consenso del bambino sono stati concessi per 22934 (84-0%) bambini (78-8% nel gruppo standard e 89-6% nel gruppo Peek), di cui 20863 (91-0%) sono stati valutati durante un periodo di 2 settimane (grafico 3).Figura 2Posizione delle scuole primarie in ciascun gruppo di studio nella Contea di Trans Nzoia, in relazione all’ospedale di Kitale, KenyaFigura 3Profilo di provaTabella 2Caratteristiche di base delle scuole e dei partecipanti allo studioGruppo di PeekGruppostandardNumerodiscuole252525Numeromedio di bambini per scuola, n (range)423 (223-1135)411 (270-1037)Distanza media dalla scuola all’ospedale di Kitale, km (range)21-1 (1-9-50-6)19-0 (1-8-37-6)Numero di bambini esaminati1057910284Sesso maschile5303 (50%)4953 (48%)Età media, anni (SD)11-2 (2-8)11-4 (2-7)Anni primari inferiori 1-33744 (35%)3236 (32%)Anni primari superiori 4-86835 (65%)7048 (69%)I dati sono n (%), salvo diversa indicazione.
In questo studio, 531 (5%) di 10579 bambini del gruppo Peek e 366 (4%) di 10284 bambini del gruppo standard non hanno superato il test di screening. Di questi 897 bambini referenziati, 379 (42%) erano maschi, con un’età media di 11-6 anni (2-9), e 273 (30%) erano nel gruppo primario inferiore; le caratteristiche erano simili tra i gruppi (tabella 3).Tabella 3Proporzione di bambini con disabilità visiva e proporzione di bambini che si sono presentati all’ospedale (esito primario)Gruppo PeekGruppoStandardGruppoStandardBambinicon disabilità visiva allo screening riferiti all’ospedale*Numerodi bambini531 (5%)366 (4%)Sesso maschile226 (43%)153 (42%)Età media, anni (SD)11-5 (3-0)11-7 (2-8)Anni primari inferiori 1-3179 (34%)94 (26%)Anni primari superiori 4-8352 (66%)272 (74%)Bambini con problemi di vista durante lo screening che hanno presentato in ospedale*Numerodi bambini285 (54%)82 (22%)Sesso maschile130 (46%)35 (43%)Età media, anni (SD)11-6 (2-9)11-5 (2-6)Anni primari inferiori 1-388 (31%)16 (20%)Anni primari superiori 4-8197 (69%)66 (72%)Bambini che non hanno potuto vedere 6/12 in uno dei due occhi nel test di acuità visiva dell’ospedaleNumerodi bambini68 (25%) 276† 37 (47%) 78‡ I dati sono n (%), se non diversamente specificato.*La menomazione della vista definita come visione inferiore a 6/12 in uno dei due occhi.†La visione di nove bambini non è stata registrata.‡La visione di quattro bambini non è stata registrata.
Dei 366 bambini riferiti dal gruppo standard, 82 (22%) sono stati presentati all’ospedale durante il periodo di follow-up di 8 settimane rispetto ai 285 (54%) di 531 bambini riferiti dal gruppo Peek. Dopo l’adattamento per il clustering scolastico, i bambini riferiti con il sistema di salute degli occhi della scuola Peek erano più propensi a frequentare l’ospedale entro 8 settimane rispetto ai bambini riferiti con il sistema di screening standard (OR 7-35 [95% CI 3-49-15-47]; p<0-0001). Quando anche la distanza dall’ospedale, l’età, il livello di istruzione e il sesso sono stati corretti, l’effetto stimato è stato simile (corretto OR 8-27 [95% CI 3-77-18-1]; p<0-0001).
Il tasso di frequenza ospedaliera tra coloro che sono risultati positivi al test per i danni alla vista è stato significativamente più alto nel gruppo Peek rispetto al gruppo standard (HR 2-56 [95% CI 1-43-4-56]; p=0-0001; figura 4; tabella 4). Tuttavia, poiché i pericoli non erano proporzionali (p<0-0001), il tempo è stato suddiviso in sezioni settimanali e l’HR è stato stimato per ogni settimana (tabella 4). Questa stima delle risorse umane è stata possibile solo per le prime 4 settimane di follow-up perché dopo questo periodo non sono arrivati in ospedale bambini del gruppo standard. Non abbiamo trovato un effetto di intervento nella prima settimana (HR 1-03 [95% CI 0-54-1-98]; p=0-92). Tuttavia, nella seconda settimana, l’evidenza suggerisce che i bambini che hanno fatto riferimento a Peek hanno avuto un tasso di frequenza aumentato, con un HR stimato di 4-63 (95% CI 2-15-9-95; p=0-0001). Effetti di intervento più forti sono stati osservati nelle settimane 3 (HR 5-01 [95% CI 2-00-12-52]; p=0-0006) e 4 (HR 11-51 [2-41-54-93]; p=0-002).Figura 4Kaplan-Meier analisi del tempo dallo screening alla frequenza alla clinica oftalmologica ospedalieraSMS=servizio messaggi brevi.Tabella 4Bambini che hanno frequentato l’ospedale dopo il ricovero iniziale durante ogni settimana del trialPeekgroupStandardgroupHazardratio (95% CI)p valueWeek191 (17%)54 (15%)1-03 (0-54-1-98)0-9232Week 2105 (37%)17 (19%)4-63 (2-15-9-95)0-0001Settimana 346 (46%)9 (22%)5-01 (2-00-12-52)0-0006Settimana 420 (49%)2 (22%)11-51 (2-41-54-93)0-0022Settimana 55 (50%)0 (22%)….Settimana 66 (51%)0 (22%)….Settimana 76 (53%)0 (22%)…..Settimana 86 (54%)0 (22%)…..I dati sono il numero di figli (% cumulativo), salvo diversa indicazione.
Dei bambini riferiti da scuole del gruppo standard, 37 (47%) di 78 bambini hanno confermato di avere problemi alla vista (quattro avevano dati di acuità visiva mancanti) rispetto a 68 (25%) di 276 bambini riferiti da scuole del gruppo Peek (nove avevano dati di acuità visiva mancanti; tabella 5). Una percentuale più alta di falsi positivi è stata identificata tra i bambini sottoposti a screening con Peek rispetto a quelli sottoposti a screening standard (p<0-0001). Tuttavia, il numero assoluto di bambini ipovedenti confermati era più alto nel gruppo Peek (n=68) rispetto al gruppo standard (n=37). La maggior parte dei bambini riferiti che non sono stati trovati con problemi alla vista in clinica ha avuto una diagnosi di congiuntivite allergica (139 [67%] di 208 bambini nel gruppo Peek e 32 [78%] di 41 bambini nel gruppo standard; tabella 5). A tutti i bambini che avevano un errore di rifrazione visivamente significativo (<6/12) sono stati offerti gratuitamente degli occhiali e tre bambini sono stati sottoposti a un intervento di cataratta.Tabella 5 Stato dell’acuità visiva e diagnosi dei bambini che sono risultati positivi all’esame di deficit visivo e che hanno poi frequentato ilgruppo ospedalieroPeekGruppostandardAcuità visiva tra i bambini che hanno frequentatol’ospedaleBambini in ogni gruppo276*78†. 6/12 o meglio in entrambi gli occhi208 (75%)41 (52%)Peggio di 6/12 in entrambi gli occhi (menomazione visiva confermata)68 (25%)37 (47%)Acuità visiva nel peggior occhio vedente dei bambini senza menomazione visiva in ospedaleBambini inogni gruppo208416/53 (1%)06/6107 (51%)23 (56%)6/966 (32%)13 (32%)6/1232 (15%)5 (12%)Diagnosi tra i bambini senza disabilità visiva in ospedaleBambiniin ogni gruppo20841Occhi normali7 (3%)1 (2%)Congiuntivite allergica, compreso il cherato-congiuntivite139 (67%)32 (78%)Errore di rifrazione21 (10%)4 (10%)Altri5 (2%)0Non dichiarato36 (17%)4 (10%)Acutezza visiva nell’occhio peggiore dei bambini con deficit visivo (in unodeidue occhi) in ospedaleBambinidi ogni gruppo68376/1819 (28%)14 (38%)6/2413 (19%)7 (19%)6/368 (12%)4 (11%)6/609 (13%)3 (8%)5/60 o peggio19 (28%)9 (24%)Diagnosi tra i bambini con disabilità visiva (in uno dei due occhi) in ospedaleBambinidi ogni gruppo6837Congiuntivite allergica, compresa la cherato-congiuntivite vernale-congiuntivite6 (9%)3 (8%)Errore di rifrazione31 (46%)26 (70%)Cicatrici corneali4 (6%)2 (5%)Anomalie del globo9 (13%)3 (8%)Cataratta2 (3%)1 (3%)Altri8 (12%)1 (3%)Non dichiarato8 (12%)1 (3%)I dati sono n (%).*Non è stata registrata la visione di nove bambini.†Non è stata registrata la visione di quattro bambini.
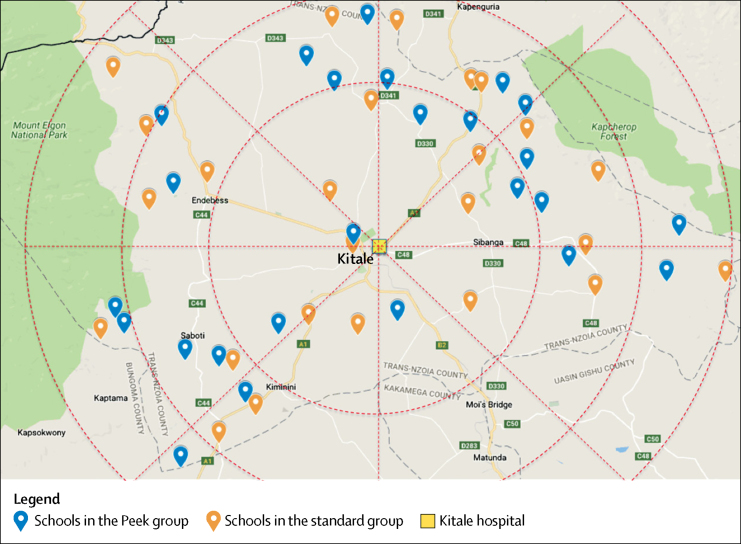
Grafico 2.Ubicazione delle scuole primarie in ogni gruppo di studio nella Contea di Trans Nzoia, in relazione all’ospedale di Kitale, Kenya
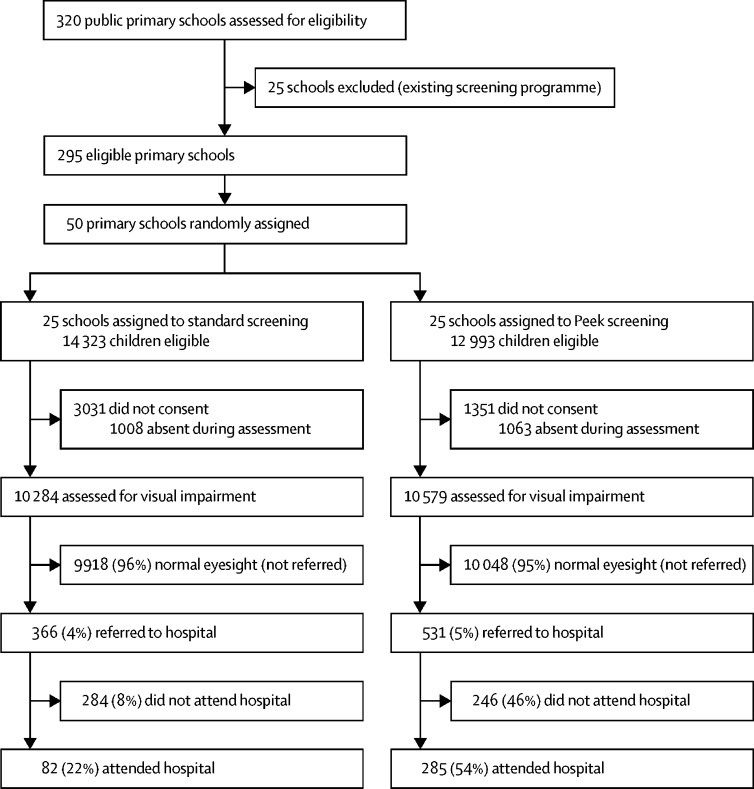
Figura 3.Profilo di prova
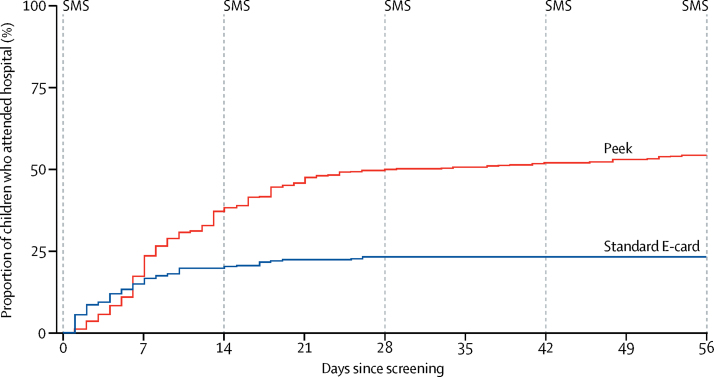
Figura 4.Analisi Kaplan-Meier del tempo dallo screening alla frequenza alla clinica oftalmologica dell’ospedaleSMS=servizio messaggi brevi.
Discussione
L’identificazione precoce e la gestione della disabilità visiva nei bambini è importante per consentire la partecipazione all’educazione e alla società.10 Abbiamo dimostrato che un sistema integrato che comprende un test di acuità visiva basato su smartphone (Peek Acuity), una scheda di riferimento stampata che illustra il grado di menomazione visiva e promemoria SMS (cioè il sistema di salute degli occhi della scuola Peek) ha migliorato significativamente il tasso complessivo di frequenza ospedaliera tra i bambini riferiti rispetto al sistema standard. In questa prima prova, per valutare l’uso degli smartphone per lo screening della vista e il referral, abbiamo scoperto che il test può essere efficacemente consegnato dagli insegnanti della scuola.
Il tasso di frequenza degli ospedali era inizialmente simile in entrambi i gruppi. Tuttavia, nel gruppo standard la frequenza del gruppo è rallentata dopo la prima settimana prima di fermarsi completamente dopo 4 settimane. L’iniziale frequenza simile in entrambi i gruppi potrebbe essere dovuta a chi ha risposto precocemente e chiede più velocemente assistenza medica. La frequenza in ospedale è stata mantenuta meglio nel gruppo Peek. Poiché il sistema Peek è un pacchetto di intervento che comprende sia SMS ripetuti che una speciale scheda di riferimento che illustra i problemi visivi, non si conoscono gli elementi che hanno portato all’aumento delle presenze. I messaggi di promemoria non sembravano avere alcun effetto aggiuntivo sulle presenze dopo l’invio dei primi due promemoria(figura 4).
Nello studio di validazione, abbiamo trovato che la sensibilità di Peek e delle carte E standard nel rilevare l’acuità visiva inferiore a 6/12 è di circa il 75% se utilizzate dagli insegnanti della scuola, rispetto a circa il 100% per il grafico ETDRS LogMAR utilizzato da un medico. La maggior parte dei falsi negativi aveva un’acuità visiva EDTRS LogMAR vicino al livello di soglia. I valori predittivi negativi di entrambi i test erano molto elevati.
La specificità e il valore predittivo positivo sono stati inferiori per Peek rispetto al sistema standard, con il risultato che sono stati indirizzati più bambini che non sono stati successivamente trovati con disabilità visive. Tuttavia, molti di loro sono stati riscontrati con una condizione oculare. Un basso valore predittivo positivo potrebbe sovraccaricare il sistema sanitario di rinvii e costi non necessari, con conseguente aumento della pressione sui servizi di assistenza oculistica limitati.12 Questi risultati falsi positivi potrebbero essere sorti per una serie di ragioni: sottili variazioni nell’angolo dello schermo dello smartphone, riflessi fuori dallo schermo o variazioni, e un aumento dell’abbagliamento da uno schermo luminoso in presenza di condizioni oculari infiammatorie, come la congiuntivite allergica.23
Per ridurre la percentuale di falsi positivi, proponiamo ulteriori strategie di test. Ciò comporta la necessità di testare nuovamente la visione di tutti i bambini che sono risultati inizialmente positivi. Un rinvio si attiva solo se il bambino non raggiunge la soglia di acuità del test ripetuto. Se un bambino non supera il primo test e poi supera il secondo, viene eseguito un terzo test di screening (massimo tre test per occhio). Il rinvio viene attivato alla conferma di due dei tre test non riusciti. Un approccio alternativo, attualmente in fase di test, prevede l’estensione del numero di optotipi mostrati per confermare il livello di acuità. Inoltre, un numero prestabilito di bambini che superano il test di screening sarà sollecitato dall’esaminatore a consegnare un test ripetuto per consentire il monitoraggio dei tassi di falsi negativi.
Questo test suggerisce che, per ogni 10.000 bambini sottoposti a screening con metodi standard, 80 di questi dovrebbero essere indirizzati a frequentare la clinica ospedaliera-38 con disabilità visiva e 42 senza. Con il sistema Peek, 269 bambini dovrebbero frequentare l’ospedale-66 con disabilità visive e 203 senza. Pertanto, con l’utilizzo della prima iterazione del sistema di salute degli occhi della scuola Peek, si prevede che altri 28 bambini ipovedenti si presenteranno alla clinica per la valutazione e il trattamento per ogni 10.000 bambini sottoposti a screening. Ciò comporta il costo di altri 161 bambini senza disabilità visive che si presentano sulla base dei metodi utilizzati in questo studio.
Le misurazioni dell’acuità visiva nei bambini ricoverati in ospedale sono state effettuate con un grafico di Snellen diversi giorni o settimane dopo la valutazione iniziale; pertanto, l’acuità visiva potrebbe aver oscillato, tenendo conto di alcune delle differenze. In precedenza è stata segnalata una variazione da breve a medio termine del test di prova dell’acuità visiva.24, 25 L’acutezza visiva viene solitamente fornita come test continuo da grandi a piccoli angoli di risoluzione. Tuttavia, le decisioni per il rinvio sono prese sulla base di una soglia da quel test continuo, <6/12. Per ragioni pratiche, dato il volume di bambini che vengono sottoposti a screening e la necessità di una decisione di rinvio piuttosto che di un punteggio di acuità che è il principale driver, un test di soglia di acuità è appropriato per lo screening. La maggior parte dei test di acuità ha una tolleranza di una linea (cioè, limiti di accordo) e quindi l’esecuzione di un test di soglia è suscettibile di portare a referti inferiori o superiori a quelli di coloro la cui acuità reale scende al di sopra o al di sotto della soglia.
Da notare che la maggior parte di questi falsi positivi per i disturbi della vista sono stati riscontrati con una certa patologia oculare, la più frequente delle malattie oculari allergiche, che è particolarmente comune in questa popolazione. Il rischio di sovraccaricare il sistema sanitario potrebbe essere ridotto con l’erogazione di servizi di triage all’interno o nelle vicinanze della scuola per esaminare tutti i bambini che sono risultati positivi e per gestire i disturbi oculari minori e, dove la capacità lo consente, la valutazione e l’erogazione di servizi di rifrazione riferendosi solo a coloro che necessitano di ulteriori cure ospedaliere in seguito alle cure secondarie. Una fase di triage diretto all’ospedale o un’ulteriore fase di triage richiedono entrambi di bilanciare la capacità del servizio di assistenza con le richieste del servizio sanitario per quella popolazione.
Una delle principali limitazioni del sistema attuale è la bassa specificità dell’algoritmo di test di soglia. Nel nostro precedente studio sugli adulti,26 abbiamo trovato una specificità sostanzialmente più alta per i gravi danni alla vista utilizzando un’acuità visiva completa in contrapposizione ad un algoritmo di prova dell’acuità di soglia, suggerendo che le modifiche all’algoritmo di prova potrebbero migliorare questo risultato. Un sistema per la salute degli occhi a scuola in due fasi, che prevede lo screening nella scuola e i servizi di triage forniti all’interno o nelle vicinanze della scuola, potrebbe ottimizzare i benefici del suo utilizzo, riducendo al minimo il potenziale sovraccarico del sistema sanitario. Questo sistema è stato successivamente perfezionato sulla base dei risultati di questa sperimentazione ed è stato implementato per sostenere servizi completi di salute degli occhi dei bambini in tutte le scuole elementari pubbliche della contea di Trans Nzoia (n=340) in collaborazione con i Ministeri della Salute e dell’Istruzione. Il sistema di triage per la raccomandazione dei servizi di rifrazione è stato sviluppato in un’iterazione del sistema che è stato implementato con successo in Botswana ed è ora in fase di preparazione per uno scale-up a livello nazionale. Sono necessarie ulteriori ricerche per valutare sistematicamente le barriere che ostacolano l’accesso ai servizi oculistici per i bambini e per sviluppare e testare misure contestualmente rilevanti per migliorare tali barriere, come dimostrato dalla sperimentazione del sistema di salute degli occhi delle scuole Peek in India.27
In conclusione, il sistema di salute degli occhi della scuola Peek ha portato a un sostanziale aumento della percentuale di bambini che hanno frequentato la clinica ospedaliera per la valutazione dopo lo screening positivo per la disabilità visiva e ha fornito visibilità in tempo reale al sistema sanitario. Questo risultato indica il valore potenziale di questa tecnologia per migliorare l’adozione dei servizi e incoraggiare il miglioramento della prestazione attraverso l’identificazione delle aree con potenziali colli di bottiglia nel percorso di cura (come le regioni con il maggior numero di bambini che non hanno frequentato l’ospedale). L’algoritmo di screening Peek Acuity utilizzato in questo trial è stato meno specifico della carta Tumbling-E nell’identificazione dei bambini con disabilità visive. Inoltre, è necessario un lavoro continuo per perfezionare ulteriormente l’algoritmo di test, mantenendo la sensibilità e migliorando la specificità senza aumentare sostanzialmente il tempo di test e riducendo sistematicamente le barriere alla cura del paziente in tutto il percorso di cura del paziente.
References
- Toledo CC, Paiva AP, Camilo GB, Maior MR, Leite IC, Guerra MR. Early detection of visual impairment and its relation to academic performance. Rev Assoc Med Bras. 2010; 56:415-419. PubMed
- Centers for Disease Control and Prevention. Economic costs associated with mental retardation, cerebral palsy, hearing loss, and vision impairment—United States, 2003. MMWR Morb Mortal Wkly Rep. 2004; 53:57-59. PubMed
- Pascolini D, Mariotti SP. Global estimates of visual impairment: 2010. Br J Ophthalmol. 2012; 96:614-618. PubMed
- WHO. WHO: Geneva; 2014. Publisher Full Text
- Barasa E, Otieno SA, Karimurio J. The prevalence and pattern of visual impairment and blindness among Primary School pupils in Kitale Municipality, Kenya. JOECSA. 2013; 17:66-69.
- Muma M, Kimani K, Kariuki W. Prevalence of refractive errors in primary school children of a rural district of Kenya. JOECSA. 2013; 13:48-51.
- Murthy GV, Gupta SK, Ellwein LB. Refractive error in children in an urban population in New Delhi. Invest Ophthalmol Vis Sci. 2002; 43:623-631. PubMed
- He M, Zeng J, Liu Y, Xu J, Pokharel GP, Ellwein LB. Refractive error and visual impairment in urban children in southern china. Invest Ophthalmol Vis Sci. 2004; 45:793-799. PubMed
- Gilbert C, Foster A. Childhood blindness in the context of VISION 2020—the right to sight. Bull World Health Organ. 2001; 79:227-232. PubMed
- Stewart-Brown SL, Haslum M. Screening of vision in school: could we do better by doing less?. BMJ. 1988; 297:1111-1113. PubMed
- Ministry of Education, Republic of Kenya. Ministry of Education: Nairobi; 2009.
- Syed A, Polack S, Eusebio C. Predictors of attendance and barriers to cataract surgery in Kenya, Bangladesh and the Philippines. Disabil Rehabil. 2013; 35:1660-1667. PubMed
- Bastawrous A, Armstrong MJ. Mobile health use in low- and high-income countries: an overview of the peer-reviewed literature. J R Soc Med. 2013; 106:130-142. PubMed
- Deloitte, Groupe Speciale Mobile Association. Groupe Speciale Mobile Association: London; 2012.
- Free C, Phillips G, Watson L. The effectiveness of mobile-health technologies to improve health care service delivery processes: a systematic review and meta-analysis. PLoS Med. 2013; 10:e1001363. PubMed
- Bastawrous A, Rono HK, Livingstone IT. Development and validation of a smartphone-based visual acuity test (peek acuity) for clinical practice and community-based fieldwork. JAMA Ophthalmol. 2015; 133:930-937. PubMed
- Lodhia V, Karanja S, Lees S, Bastawrous A. Acceptability, usability, and views on deployment of peek, a mobile phone mhealth intervention for eye care in Kenya: qualitative study. JMIR mHealth uHealth. 2016; 4:e30. PubMed
- Campbell MK, Piaggio G, Elbourne DR, Altman DG. Consort 2010 statement: extension to cluster randomised trials. BMJ. 2012; 345:e5661. PubMed
- Raab GM, Butcher I. Balance in cluster randomized trials. Stat Med. 2001; 20:351-365. PubMed
- Carter BR, Hood K. Balance algorithm for cluster randomized trials. BMC Med Res Methodol. 2008; 8:65. PubMed
- Gilbert C, Foster A, Negrel AD, Thylefors B. Childhood blindness: a new form for recording causes of visual loss in children. Bull World Health Organ. 1993; 71:485-489. PubMed
- Schoenfeld D. Partial residuals for the proportional hazards regression model. Biometrika. 1982; 69:239-241.
- Black JM, Jacobs RJ, Phillips G. An assessment of the iPad as a testing platform for distance visual acuity in adults. BMJ Open. 2013; 3:e002730.
- Siderov J, Tiu AL. Variability of measurements of visual acuity in a large eye clinic. Acta Ophthalmol. 1999; 77:673-676.
- Arditi A, Cagenello R. On the statistical reliability of letter-chart visual acuity measurements. Invest Ophthalmol Vis Sci. 1993; 34:120-129. PubMed
- Bastawrous A, Giardini ME, Bolster NM. Clinical validation of a smartphone-based adapter for optic disc imaging in Kenya. JAMA Ophthalmol. 2016; 134:151-158. PubMed
- Morjaria P, Bastawrous A, Murthy GV, Evans J, Gilbert C. Effectiveness of a novel mobile health education intervention (Peek) on spectacle wear among children in India: study protocol for a randomized controlled trial. Trials. 2017; 18:168. PubMed
Fonte
Rono HK, Bastawrous A, Macleod D, Wanjala E, DiTanna G, et al. (2018) Smartphone-based screening for visual impairment in Kenyan school children: a cluster randomised controlled trial. The Lancet. Global Health 6(8): . https://doi.org/10.1016/S2214-109X(18)30244-4





